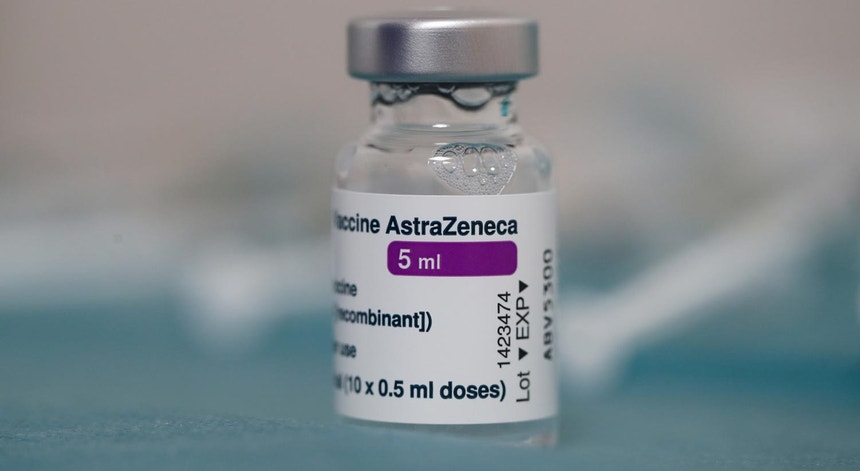
Cerca de 40 milhões de doses de vacinas anti-Covid-19 fabricadas pela AstraZeneca permanecem armazenadas nos Estados Unidos, sem qualquer destino. Enquanto isso, dezenas de países onde a vacina já foi autorizada esperam e desesperam por fornecimentos.
Após diversos percalços, a AstraZeneca continua à espera de testes clínicos que autorizem a comercialização da vacina no país e está a tentar usar as doses entretanto produzidas para cumprir contratos atrasados com outros Governos.
Só que as autoridades norte-americanas franzem o sobrolho.
O debate sobre o que fazer a todas estas doses tem sido aceso na Casa Branca e entre responsáveis federais, e incluiu a própria empresa britânico-sueca. De um lado da barricada estão os que afirmam que a Administração Biden deveria autorizar a exportação, do outro aqueles que não querem abrir mão das vacinas.
Gonzalo Viña, um porta-voz da AstraZeneca,confirmou ao New York Times que "vários países e Governos contactaram a Administração norte-americana sobre a doação das doses e apelámos o Governo dos EUA a considerar cuidadosamente estes pedidos".
Um pedido endereçado pela AstraZeneca à Casa Branca no sentido de poder dispor das doses para cumprir contratos com União Europeia terá sido sumariamente recusado, adianta o NYT citando fontes oficiais sob anonimato.
A Agência Reuters avançou também esta sexta-feira que Washington já avisou a UE de que não vai autorizar o envio das vacinas da AstraZeneca produzidas no país, de acordo com um documento que circula em Bruxelas e a que a agência teve acesso. Considerada inicialmente uma das favoritas à autorização nos EUA por ser mais barata e mais fácil de armazenar por longos períodos do que outras, a vacina da AstraZeneca, produzida com a Universidade de Oxford, terá acabado por encalhar numa série de problemas burocráticos e de falta de documentação que atrasaram os processos de verificação.
As hesitações do Governo norte-americano quanto ao que fazer com as vacinas, estarão relacionadas com a incerteza de poder cumprir promessas do Presidente Joe Biden, de que até finais de maio o país teria doses suficientes para inocular todos os adultos nos Estados Unidos.
Alguns responsáveis federais têm pressionado a Casa Branca a decidir nas próximas semanas, sobre o envio destas vacinas para o Brasil, para a União Europeia ou para o Reino Unido.
"Se estas doações fossem autorizadas, iríamos pedir a Administração instruções quanto à sua reposição para uso nos Estados Unidos", afirmou Viña ao NYT.
A AstraZeneca só pôde comprometer-se em fevereiro a fornecer à UE 34 milhões de vacinas no primeiro trimestre de 2021, um terço dos 90 milhões inicialmente contratados, quando tem 40 milhões bloqueadas nos EUA.
A maior parte, 30 milhões, estão armazenadas no Ohio, à espera do fill-finish, a etapa final de todo o processo na qual a vacina é colocada nos frascos de expedição, referiu ao NYT outro responsável a par do sistema.
Outros 10 milhões, encomendados pela AstraZeneca à Bio Solutions, esperam igualmente em Baltimore o fill-finish e o empacotamento.
Receios e recuosAlém de ter a vacina parada após os custos de produção e de não conseguir cumprir contratos, a empresa está a enfrentar uma onda de publicidade negativa devido a alegados efeitos secundários da sua vacina. Foi observada a formação de coágulos sanguíneos e hemorragias em 30 dos cinco milhões de pessoas inoculadas na Europa com a vacina da AstraZeneca. No Reino Unido, 41 pessoas entre 11 milhões que receberam a vacina registaram anafilaxia e hipersensibilidade (reações alérgicas).
Autorizada inicialmente em 70 países - incluindo o Brasil, que lhe deu luz verde definitiva precisamente esta sexta-feira apesar dela já estar a ser ministrada no país desde finais de janeiro - a vacina da AstraZeneca foi suspensa numa dezena, por precaução, com outros, como a República Democrática do Congo, a atrasarem a sua administração.
A Agência Europeia do Medicamento (EMA) disse quinta-feira que está a investigar o problema das tromboembolias, mas que considera à mesma a vacina segura. "As vantagens da vacina permanecessem superiores aos riscos", constatou, ecoada esta sexta-feira pela França.
A EMA anunciou entretanto que a possibilidade de alergias graves observada no Reino Unido deverá ser acrescentadas à lista dos possíveis efeitos secundários.
Outros países receiam que a baixa eficácia da vacina (70%) contra o vírus inicial e falta de dados face às variantes que surgiram entretanto, signifique que não há necessidade de investir nela.
Sem "provas de risco" agravado
Esta tarde, a AstraZeneca defendeu a integridade e segurança da sua vacina contra a Covid-19.
Não há "qualquer prova de risco agravado" de que esta provoque coágulos sanguíneos, referiu em comunicado. "De facto, os números quanto a este tipo (de problema) são muito inferiores entre os indivíduos vacinados comparativamente ao expectável na população em geral", afirmou a empresa.
A OMS disse também hoje que "não há qualquer razão para não utilizar" a vacina contra a Covid-19 produzida pela AstraZeneca, fazendo notar que os seus especialistas se tinham debruçado sobre a questão sanguínea sem até agora ter sido descortinada qualquer ligação causa-efeito entre estes e a vacina.
Um porta-voz da organização sublinhou também que até 9 de março foram ministradas 268 milhões de doses de vacinas contra a Covid-19 em todo o mundo, "sem que até àquela data se tivesse registado uma única morte ligada à sua administração". Em Itália, contudo, um homem de 50 anos faleceu após desenvolver uma trombose venosa profunda.
Por ser mais barata de produzir e de armazenar do que a sua rival da Pfizer-BioNTech, a vacina da AstraZeneca constitui o tronco principal dos programas de vacinação apoiados pelo Covax, o sistema de distribuição a países mais pobres implementado pela OMS, apesar da sua eficácia mais baixa em laboratório e falta de garantias de combate às novas variantes do SARS-CoV-2.